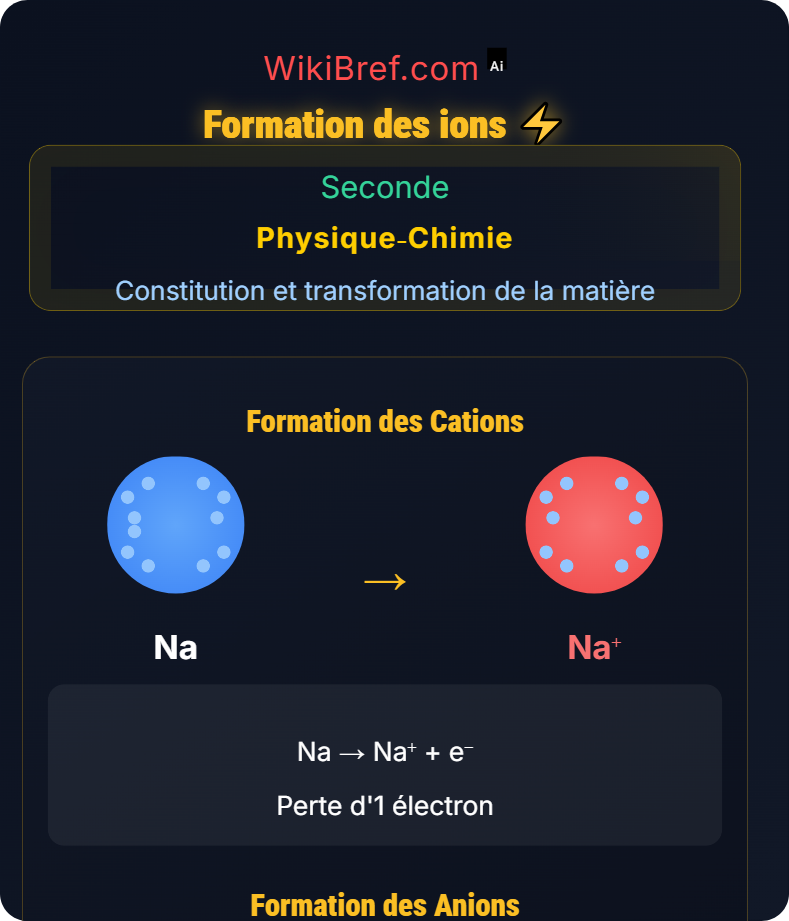
Formation des ions
\( \text{Atome} \rightarrow \text{Ion} + \text{électrons} \)
Perte ou gain d'électrons de valence
Noyau
Na
+1e⁻
→ Na⁺
→
Cl
+1e⁻
→ Cl⁻
Cations communs
Na⁺ (sodium), Ca²⁺ (calcium)
Mg²⁺ (magnésium), Al³⁺ (aluminium)
Mg²⁺ (magnésium), Al³⁺ (aluminium)
Anions communs
Cl⁻ (chlorure), O²⁻ (oxyde)
S²⁻ (sulfure), F⁻ (fluorure)
S²⁻ (sulfure), F⁻ (fluorure)
Types d'ions
Cation : atome qui perd des électrons
Anion : atome qui gagne des électrons
Charge = protons - électrons
Recherche de configuration stable
Règles de stabilité
Règle du duet (2e⁻) : H, Li, Be
Règle de l'octet (8e⁻) : C, N, O, F, Ne
Similaire à gaz nobles
Exemples de réactions
\( \text{Na} \rightarrow \text{Na}^+ + e^- \)
\( \text{Cl} + e^- \rightarrow \text{Cl}^- \)
Formation de NaCl (chlorure de sodium)
Conseils & Astuces
Métaux forment des cations
Non-métaux forment des anions
Électrons de valence se trouvent à l'extérieur
Charge de l'ion dépend de la colonne du tableau
Groupe 1 → charge +1, Groupe 17 → charge -1
Erreurs Fréquentes
Erreur 1 :
Confondre cation et anion
Erreur 2 :
Oublier que la charge dépend des électrons de valence
Erreur 3 :
Croire que tous les électrons sont concernés
Applications
Solutions ioniques :
Conducteurs d'électricité
Électrolytes dans le corps
Électrolytes dans le corps
Composés ioniques :
Sel de table (NaCl)
Calcaire (CaCO₃)
Calcaire (CaCO₃)