Structure de l'atome
\( Z = \text{nombre de protons} \)
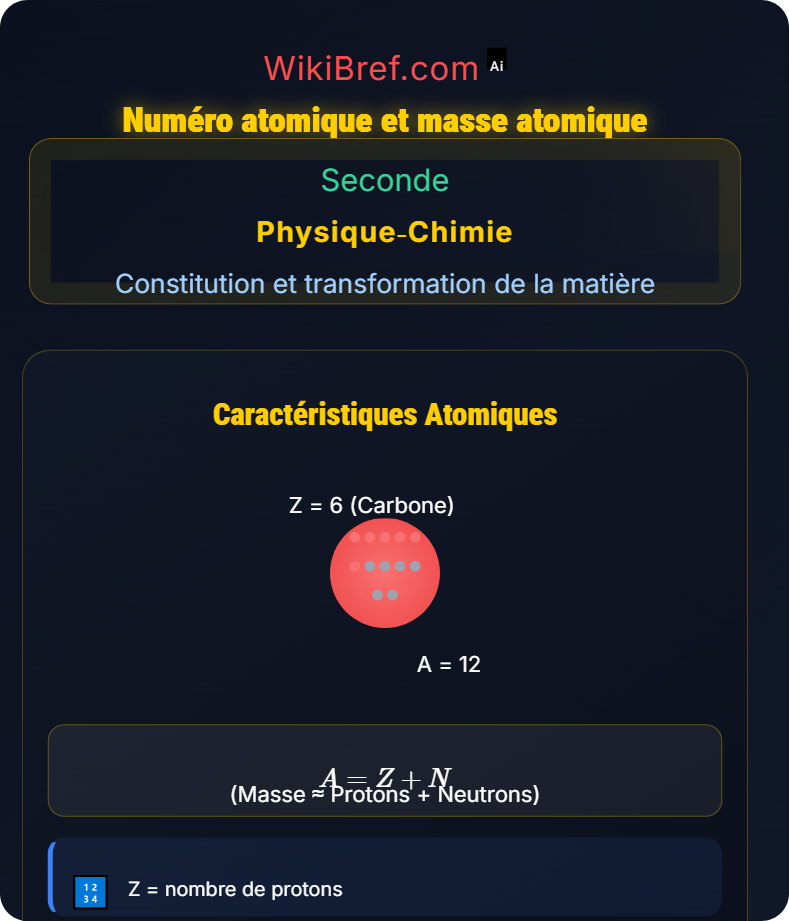
\( A = Z + N \)
Z: numéro atomique, A: nombre de masse, N: neutrons
Exemple Hydrogène:
Z = 1 (1 proton)
A = 1 (1 proton)
Neutrons = 0
A = 1 (1 proton)
Neutrons = 0
Exemple Carbone:
Z = 6 (6 protons)
A = 12 (6 protons + 6 neutrons)
Neutrons = 6
A = 12 (6 protons + 6 neutrons)
Neutrons = 6
Numéro atomique (Z)
Z = nombre de protons dans le noyau
Détermine l'élément chimique
Identité unique de chaque élément
Égal au nombre d'électrons dans l'atome neutre
Masse atomique (A)
A = Z + nombre de neutrons
Nombre total de nucléons
Mesure approximative de la masse
Conseils & Astuces
Z identifie l'élément chimique
Tous les atomes de même Z sont du même élément
A représente la somme des protons et neutrons
Les isotopes ont même Z mais différent A
Notation: AZX
Erreurs Fréquentes
Erreur 1 :
Confondre Z et A
Erreur 2 :
Penser que tous les atomes d'un élément ont le même A
Erreur 3 :
Oublier que Z détermine l'identité chimique