Principe fondamental
Conservation des atomes
Les atomes ne sont ni créés ni détruits
H₂ + O₂
→
H₂O
2H₂ + O₂
→
2H₂O
Avant équilibrage :
1 H₂ → 2 atomes H
1 O₂ → 2 atomes O
1 H₂O → 2 atomes H, 1 atome O
1 O₂ → 2 atomes O
1 H₂O → 2 atomes H, 1 atome O
Après équilibrage :
2 H₂ → 4 atomes H
1 O₂ → 2 atomes O
2 H₂O → 4 atomes H, 2 atomes O
1 O₂ → 2 atomes O
2 H₂O → 4 atomes H, 2 atomes O
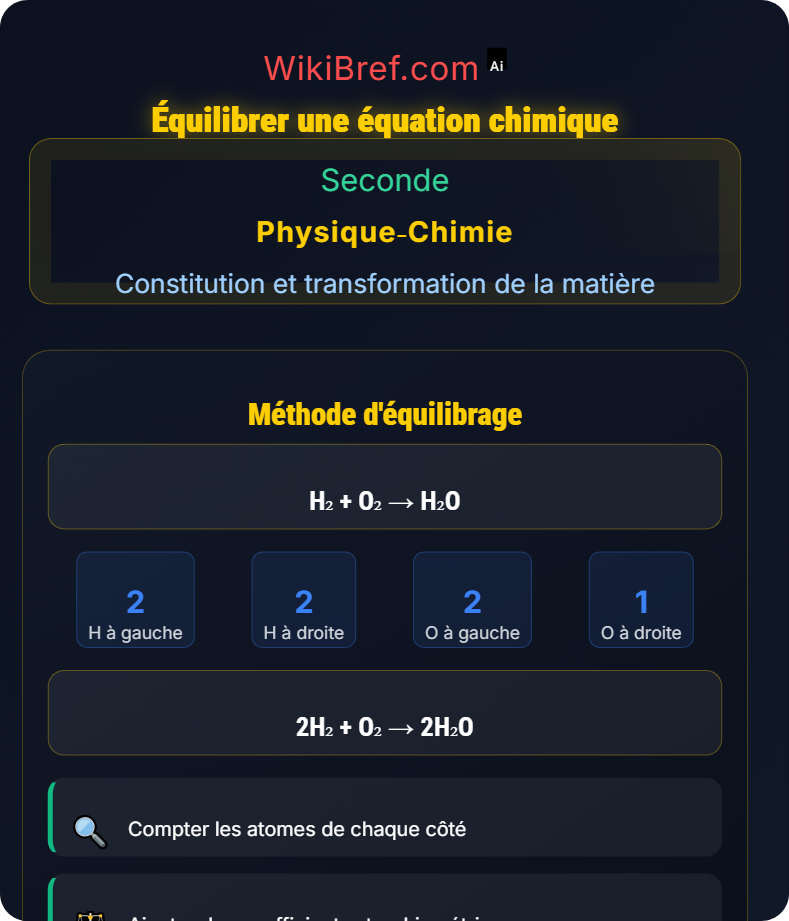
Méthode d'équilibrage
Identifier tous les atomes
Compter les atomes de chaque côté
Placer des coefficients devant les molécules
Vérifier que les atomes sont équilibrés
Exemple détaillé
CH₄ + O₂ → CO₂ + H₂O
CH₄ + 2O₂ → CO₂ + 2H₂O
1C, 4H, 4O → 1C, 4H, 4O
Conseils & Astuces
Commencer par les atomes qui n'apparaissent qu'une fois de chaque côté
Ne jamais modifier les indices dans les formules chimiques
Les coefficients doivent être des nombres entiers
Utiliser un tableau pour compter les atomes
Vérifier l'équilibre pour chaque élément chimique
Erreurs fréquentes
Erreur 1 :
Changer les indices au lieu des coefficients
Erreur 2 :
Oublier de vérifier tous les éléments
Erreur 3 :
Ne pas utiliser les plus petits coefficients possibles